True
2020-10-12
Insabbiata l’unica cura antivirus che funziona
iStock
L'Italia ha la terapia per salvare i malati da Covid ma non riesce ad applicarla su larga scala. È uno dei paradossi del nostro sistema sanitario. Stiamo parlando della cura con il plasma iperimmune.
È una soluzione della quale si parlò moltissimo in primavera; ora però se ne sono perse le tracce dopo il clamore iniziale. Un silenzio determinato dall'ostruzionismo di una parte della comunità scientifica, da polemiche pretestuose, nonostante gli indubbi risultati della sperimentazione. Eppure, l'Italia ha fatto da apripista, prima nel mondo occidentale ad avere una cura contro il coronavirus. Il nostro successo ha indotto numerosi Paesi ad avviare studi simili e applicare la stessa terapia: nel caso degli Stati Uniti sono stati curati 35.000 pazienti. Perfino il presidente Donald Trump è stato trattato, tra gli altri farmaci, anche con plasma iperimmune.
La cura potrebbe rivelarsi determinante dal momento che l'Europa sta esaurendo le scorte del remdesivir, l'antivirale finora più efficace usato. L'Ue è corsa ai ripari acquistando 500.000 dosi aggiuntive del medicinale approvato dall'Agenzia del farmaco europea (Ema). Lo scorso luglio gli Stati Uniti hanno fatto incetta di 500.000 dosi mentre l'Europa ne aveva prenotate 30.000. Secondo l'Aifa, l'Agenzia italiana per il farmaco, l'Italia non avrebbe problemi. La terapia con il plasma iperimmune sarebbe un sostegno fondamentale. Ma le resistenze persistono. Agli inizi di marzo, in piena emergenza, due ospedali, il Carlo Poma di Mantova e il San Matteo di Pavia, iniziano a somministrare a un certo numero di contagiati il plasma (che è la parte liquida del sangue) di persone guarite dal virus. Si partiva dall'ipotesi che indurre sufficienti livelli di anticorpi al paziente infetto avrebbe ridotto la carica virale e la severità della malattia.
È il meccanismo definito di immunizzazione passiva, noto da decenni essendo stato applicato con successo alle epidemie di ebola, aviaria, mers e certi tipi di influenza. Lo studio, iniziato il 17 marzo e concluso l'8 maggio, nel picco del contagio, ha visto l'arruolamento di 46 pazienti ricoverati nei due ospedali con difficoltà di respirazione tali da richiedere il supporto di ossigeno o l'intubazione. I medici hanno notato subito che dopo la trasfusione di plasma immune aggiunto a colture cellulari fermava lo sviluppo del virus. Era il segno della presenza di anticorpi neutralizzanti. Il risultato della sperimentazione, pubblicato su Haematologica, una delle più prestigiose riviste scientifiche del settore, è stato «superiore alle più rosee aspettative». All'inizio della sperimentazione, sulla base dei dati ministeriali, la mortalità dei pazienti in terapia intensiva era tra il 13 e il 20%. Utilizzando invece questa tecnica, si legge sulla rivista scientifica, «la mortalità si è ridotta al 6%. In altre parole, da 1 decesso atteso ogni 6 pazienti, se n'è verificato 1 ogni 16. Contemporaneamente, si constatava che anche gli altri parametri subivano miglioramenti considerevoli: i valori del distress respiratorio miglioravano entro la prima settimana e i tre parametri fissati per l'infezione diminuivano in maniera altrettanto importante. Il risultato più rilevante è quello di una riduzione della mortalità assoluta del 9%».
Questo studio è stato il primo nel mondo occidentale sull'utilizzo del plasma convalescente nella terapia anti Covid. Si apriva un concreto spiraglio di speranza. Immediatamente sui due ospedali sono arrivate richieste a valanga per avere i dettagli della terapia. Gli Stati Uniti sono stati primi a muoversi, autorizzando subito a utilizzare il plasma di soggetti in convalescenza da Covid come terapia emergenziale assieme al remdesivir. Ma in Italia la comunità scientifica si è divisa tra i fautori e i contrari. Questi ultimi hanno riesumato vecchie polemiche sui rischi dell'uso del plasma e sulla mancanza di un'evidenza scientifica definitiva, che però è possibile solo dopo una lunga sperimentazione.
Altre perplessità si aggiunsero quando apparvero ricerche come quella condotta dall'Indian council of medical research secondo cui il plasma iperimmune non riduce la mortalità Covid e non ha effetti rilevanti sul decorso della malattia: ricerche poi rivelatesi prive di fondamento scientifico. Forti critiche si abbatterono sui due ospedali lombardi. Tra gli altri, il dottor Giuseppe De Donno, primario di pneumologia a Mantova, divenne un volto noto nel difendere e spiegare la bontà del metodo. Nel frattempo, gli ospedali d'oltralpe chiamavano i colleghi di Pavia e Mantova per imparare e poter applicare la loro cura.
All'estero, dunque, la terapia lombarda va alla grande. E in Italia, che fine ha fatto? Al momento manca l'autorizzazione dell'Aifa, che arriva quando sul farmaco c'è un'evidenza scientifica definitiva. Le Regioni si muovono in ordine sparso creando banche del plasma. L'Aifa ha promosso uno studio nazionale denominato Tsunami, con l'obiettivo, come spiega alla Verità, di «valutare con opportuno rigore metodologico l'efficacia e la sicurezza della terapia. Ma non prevede in alcun modo un trattamento industriale del plasma».
A oggi hanno aderito al programma 76 centri, ma ne sono stati attivati soltanto 15 e in appena 8 sono iniziati gli arruolamenti di pazienti: 7 in Toscana più Niguarda a Milano. Dal 15 luglio, soltanto 34 pazienti sono stati trattati con questa sperimentazione; il paziente 1 è guarito in 72 ore con la comparsa di anticorpi prima mancanti. L'Aifa però ammette che «non è possibile al momento prevedere quando sarà completato l'arruolamento e quando saranno disponibili i primi dati». Per stilare una prima analisi preliminare servono 250 pazienti e per la validità scientifica bisogna arrivare a 476: così ha spiegato il dottor Francesco Menichetti, direttore dell'unità malattie infettive dell'ospedale di Pisa. Il quale conferma che, di fatto, è tutto fermo.
È molto probabile che ci vorrà ancora molto tempo per avere risultati definitivi. Come bisognerà aspettare almeno un paio d'anni per avere un farmaco. In Italia c'è un'unica azienda del settore dei plasmaderivati, tra le prime cinque al mondo, la toscana Kedrion, appartenente alla famiglia Marcucci, che potrebbe arrivare a produrre un medicinale apposito. «Stiamo lavorando a un farmaco con immunoglobuline iperimmuni. Non utilizziamo il plasma nella sua totalità ma solo gli anticorpi contenuti, che sono quindi concentrati e sterilizzati. Il farmaco potrebbe essere utilizzato anche in soggetti sani. Avrebbe una durata inferiore al vaccino, circa uno o due mesi, e i soggetti sarebbero immunizzati temporaneamente. La vaccinazione fornisce una protezione di lunga durata», spiega Alessandro Gringeri, responsabile ricerca e sviluppo di Kedrion, «ma non si può effettuare su soggetti malati o immunodepressi. Il farmaco con le immunoglobuline potrebbe servire per le emergenze, per situazioni acute o per pazienti affetti con sintomatologia lieve, che sta evolvendo». Quali sono i tempi? «Ora stiamo facendo la sperimentazione in Israele», risponde Gringeri, «in collaborazione con l'azienda israeliana Kamada e contiamo di inoltrare la richiesta di approvazione entro la fine del prossimo anno. Nel 2022 il farmaco potrebbe essere sul mercato».
«Noi abbiamo scoperto la terapia però sono gli altri ad applicarla»

Cesare Perotti
«L'Italia scopre la terapia ma poi sono gli altri che la applicano su larga scala. Mentre la comunità scientifica italiana si divideva tra favorevoli e contrari, gli Stati Uniti hanno preso la nostra terapia e, senza perdere tempo, la stanno utilizzando su tutto il territorio nazionale. Anche numerosi Paesi europei ce l'hanno chiesta». Cesare Perotti è direttore del servizio immunotrasfusionale del policlinico di Pavia, che per primo assieme all'ospedale Carlo Poma di Mantova ha sperimentato la terapia del plasma iperimmune per curare i malati da Covid.
È vero che la vostra cura è stata copiata dagli Stati Uniti?
«Il 18 marzo mi ha telefonato la presidente dell'American society of hematology. È stata molto diretta. Mi ha chiesto se potessi mandarle il protocollo che avevamo elaborato per la cura con il plasma iperimmune. Ho risposto subito. Negli Usa il programma è partito immediatamente. La Food and drug administration, l'ente governativo che regolamenta i prodotti alimentari e farmaceutici, dipendente dal Dipartimento della salute, ha autorizzato l'utilizzo del plasma di soggetti in convalescenza da Covid, come terapia emergenziale insieme al Remdesivir, un farmaco antivirale».
Quanti pazienti sono stati trattati negli Usa con la vostra cura?
«Il sito della Mayo Clinic, che coordina tutto il programma negli Stati Uniti, riporta i dati aggiornati sull'applicazione della terapia. Sono coinvolti 2.747 ospedali, 14.759 medici partecipano al programma e hanno avuto l'infusione 85.206 malati. Il presidente Donald Trump, da quanto si è saputo, è stato curato con anticorpi monoclonali alcuni ottenuti dal plasma, altri realizzati in laboratorio».
Quali altri Paesi si sono rivolti a voi?
«Il Policlinico ha dato il protocollo anche a Francia e Spagna».
Le istituzioni europee si sono mosse?
«La Commissione ha assegnato al policlinico San Matteo di Pavia e a me il coordinamento del programma del plasma convalescente per l'Europa con un finanziamento che coinvolge tutti i Paesi europei. Con il programma European blood alliance abbiamo avuto un importante riconoscimento oltre confine».
Quale è la situazione in Italia?
«Ci muoviamo tra tante polemiche. Ci hanno criticato perché quando siamo partiti a marzo non avevamo risultati randomizzati. Ma questi richiedono molto tempo e a marzo, in piena pandemia, non potevamo aspettare: dovevamo agire subito e i risultati sono stati ottimi».
Quando sarà ufficializzata la cura?
«A fine maggio è partito lo studio chiamato Tsunami, coordinato da me e dall'ospedale di Pisa. È un protocollo nazionale randomizzato, promosso dal ministero della Salute, dall'Istituto superiore di sanità e dall'Aifa, con l'obiettivo di ottenere evidenze scientifiche sul ruolo della terapia con il plasma iperimmune. Hanno aderito 76 ospedali, ma un conto è iscriversi e un altro attivarsi. Si procede lentamente. D'altronde i convalescenti a cui fare i prelievi sono diminuiti e l'arruolamento di pazienti va a rilento. Dovevamo partire prima».
Come mai non è stato attivato subito un programma nazionale?
«C'è stato un deficit di organizzazione e tante, troppe, polemiche».
A pensare male talvolta ci si indovina: non è che questa terapia, siccome ha costi ridotti, dà fastidio all'industria farmaceutica?
«Pasolini diceva: io so ma non ho le prove. Una cura con l'eparina o il desametasone che costa 2-3 euro impatta in modo diverso rispetto a un antivirale come il Remdesivir che costa circa 2.500 euro a paziente».
C'è al mondo una terapia standard per la cura del Covid?
«La risposa è no. Ci sono evidenze che alcuni approcci terapeutici vanno meglio di altri. Per la cura del Covid si usano diversi farmaci, ognuno per la sua specificità».
Ogni tanto appare uno studio che contesta l'efficacia della cura con il plasma, per esempio quello dell'Indian council of medical research.
«È uno studio che non ha alcuna validità. Hanno preso del plasma a caso, senza effettuare i test preventivi in grado di verificare se ci fossero gli anticorpi. Di che cosa stiamo parlando?».
«A Mantova le guarigioni superano il 90%»

Massimo Franchini
«Avremmo dovuto agire subito ma c'è stata una forte resistenza dovuta al pregiudizio che si porta dietro l'uso del plasma. È vero, fino a 40 anni fa poteva trasmettere l'epatite e l'Hiv, ma ora è super testato e questi rischi si sono annullati». Massimo Franchini, direttore del servizio di immunoematologia e medicina trasfusionale dell'ospedale Carlo Poma di Mantova, che per primo ha avviato la sperimentazione della terapia con il plasma iperimmune, rivela come mai in Italia la cura fa fatica a essere accettata. «A marzo e aprile ci fu molta resistenza dalla comunità scientifica. Forse ha giocato anche il solito meccanismo del campanilismo di qualche scienziato che avrebbe voluto mettere il suo nome sotto la cura. Ma i risultati ci sono. Noi siamo stati i primi nel mondo occidentale a individuare questa terapia. Il paradosso è che è stata utilizzata soltanto da pochi centri che ci hanno creduto. Adesso, in tutto il mondo, sono in corso centinaia di studi sul plasma iperimmune. In Italia invece si reagisce quasi con gioia quando esce qualche lavoro che mette in dubbio l'efficacia della terapia».
Lei è responsabile della sicurezza del plasma: come mai tanta reticenza a usare una cura che altri Paesi ci hanno copiato?
«È proprio questo il punto. Il plasma che usiamo è super sicuro, non c'è alcun rischio di trasmettere malattie infettive. Inoltre, si sa quanti anticorpi contiene come se fosse un farmaco. Calcoliamo il numero di dosi, quanto e come somministrarlo. Ma poi, basta pensare che personaggi come Trump e Berlusconi sono stati trattati con un mix di farmaci che comprendeva il cortisone come antinfiammatorio, il remdesivir come antivirale e anche una fonte di anticorpi come i monoclonali o il plasma iperimmune».
Bisognerebbe creare delle banche del plasma, ma manca una regìa pubblica e tutto è lasciato all'iniziativa degli ospedali.
«Ci sarebbe voluto un maggior coordinamento dell'Istituto superiore di sanità per la raccolta di plasma. Gli Usa sono partiti subito con la nostra terapia, tramite una task force governativa che ha promosso la raccolta di plasma su tutto il territorio nazionale. L'Italia è stata interessata precocemente dalla pandemia ma si è mossa lentamente. Ci sono banche del plasma regionali in Lombardia, Veneto, Toscana, Marche, Lazio, legate agli ospedali. L'utilizzo clinico è coordinato dallo studio Tsunami».
Quando dalla sperimentazione si passerà a un uso su larga scala?
«Sì, al momento siamo ancora alla sperimentazione. L'Aifa autorizza i farmaci e le terapie quando ci sono prove scientifiche definitive, che nel nostro caso ancora non ci sono. Per averle occorre un processo lungo che richiede tanto tempo. Ma la mia opinione è che una volta appurata la sicurezza e a fronte dei risultati ottimi della sperimentazione, perché non usarlo? Gli americani si sono posti questa domanda e, con grande pragmatismo, hanno deciso di adottare la terapia anche senza evidenze scientifiche definitive».
Avete posto questo problema all'Istituto superiore di sanità? La pandemia richiede interventi tempestivi.
«L'Istituto è stato interpellato più volte, ma secondo loro non valeva la pena di usare il plasma in modo estensivo. Hanno dubbi sull'efficacia, hanno sempre mantenuto questa linea. La storia della medicina dirà chi aveva ragione».
In attesa dell'autorizzazione degli istituti sanitari, come potete applicare la terapia?
«La cura del plasma è inserita in protocolli di studi, come lo Tsunami, o per cosiddetto uso compassionevole, cioè quando per una patologia manca un trattamento riconosciuto come definitivo ma si ritiene che un farmaco possa essere utile. Occorre l'autorizzazione del Comitato etico che noi abbiamo».
Quali risultati avete ottenuto nell'ospedale di Mantova?
«Stiamo applicando la terapia da marzo e finora abbiamo trattato 150 pazienti. Le guarigioni superano il 90%».
Ci sono requisiti affinché il plasma abbia la maggiore efficacia?
«Il plasma funziona se vengono rispettati i seguenti requisiti: deve contenere un adeguato livello di anticorpi e deve essere somministrato precocemente. Con queste condizioni la malattia si blocca e regredisce».
Avete ricevuto richieste da Paesi esteri per fornire supporto scientifico?
«Abbiamo continue richieste di collaborazioni per mettere a disposizione le nostre conoscenze. Abbiamo fornito un supporto scientifico con collegamenti Web dall'America Latina all'Albania».
Siete un competitor temibile per l'industria farmaceutica. La cura con il plasma costa poco.
«Qualcuno ci può considerare un pericoloso competitor, ma io vedo un rapporto di collaborazione e non di antagonismo con l'industria farmaceutica. La terapia migliore, al momento, è un cocktail di componenti, quali antivirali, cortisone e plasma. La produzione di un farmaco richiede tanto tempo e forse per quella data sarà già arrivato il vaccino».
Continua a leggereRiduci
Il trattamento con il plasma iperimmune ha ridotto la mortalità dal 20 al 6% a costo zero. Ma la sperimentazione avviata a marzo non piace a parte della comunità scientifica. E ora è quasi ferma.Il primo medico ad averla sperimentata: «Da noi troppe polemiche, negli Usa il programma è partito subito. Ostacolati da Big Pharma? È chiaro che ciò che costa 2 euro impatta diversamente da ciò che ne rende 2.500».«Finora abbiamo trattato 150 pazienti, i risultati ci sono e non vi sono rischi di trasmettere malattie infettive».Lo speciale contiene tre articoli.L'Italia ha la terapia per salvare i malati da Covid ma non riesce ad applicarla su larga scala. È uno dei paradossi del nostro sistema sanitario. Stiamo parlando della cura con il plasma iperimmune. È una soluzione della quale si parlò moltissimo in primavera; ora però se ne sono perse le tracce dopo il clamore iniziale. Un silenzio determinato dall'ostruzionismo di una parte della comunità scientifica, da polemiche pretestuose, nonostante gli indubbi risultati della sperimentazione. Eppure, l'Italia ha fatto da apripista, prima nel mondo occidentale ad avere una cura contro il coronavirus. Il nostro successo ha indotto numerosi Paesi ad avviare studi simili e applicare la stessa terapia: nel caso degli Stati Uniti sono stati curati 35.000 pazienti. Perfino il presidente Donald Trump è stato trattato, tra gli altri farmaci, anche con plasma iperimmune.La cura potrebbe rivelarsi determinante dal momento che l'Europa sta esaurendo le scorte del remdesivir, l'antivirale finora più efficace usato. L'Ue è corsa ai ripari acquistando 500.000 dosi aggiuntive del medicinale approvato dall'Agenzia del farmaco europea (Ema). Lo scorso luglio gli Stati Uniti hanno fatto incetta di 500.000 dosi mentre l'Europa ne aveva prenotate 30.000. Secondo l'Aifa, l'Agenzia italiana per il farmaco, l'Italia non avrebbe problemi. La terapia con il plasma iperimmune sarebbe un sostegno fondamentale. Ma le resistenze persistono. Agli inizi di marzo, in piena emergenza, due ospedali, il Carlo Poma di Mantova e il San Matteo di Pavia, iniziano a somministrare a un certo numero di contagiati il plasma (che è la parte liquida del sangue) di persone guarite dal virus. Si partiva dall'ipotesi che indurre sufficienti livelli di anticorpi al paziente infetto avrebbe ridotto la carica virale e la severità della malattia.È il meccanismo definito di immunizzazione passiva, noto da decenni essendo stato applicato con successo alle epidemie di ebola, aviaria, mers e certi tipi di influenza. Lo studio, iniziato il 17 marzo e concluso l'8 maggio, nel picco del contagio, ha visto l'arruolamento di 46 pazienti ricoverati nei due ospedali con difficoltà di respirazione tali da richiedere il supporto di ossigeno o l'intubazione. I medici hanno notato subito che dopo la trasfusione di plasma immune aggiunto a colture cellulari fermava lo sviluppo del virus. Era il segno della presenza di anticorpi neutralizzanti. Il risultato della sperimentazione, pubblicato su Haematologica, una delle più prestigiose riviste scientifiche del settore, è stato «superiore alle più rosee aspettative». All'inizio della sperimentazione, sulla base dei dati ministeriali, la mortalità dei pazienti in terapia intensiva era tra il 13 e il 20%. Utilizzando invece questa tecnica, si legge sulla rivista scientifica, «la mortalità si è ridotta al 6%. In altre parole, da 1 decesso atteso ogni 6 pazienti, se n'è verificato 1 ogni 16. Contemporaneamente, si constatava che anche gli altri parametri subivano miglioramenti considerevoli: i valori del distress respiratorio miglioravano entro la prima settimana e i tre parametri fissati per l'infezione diminuivano in maniera altrettanto importante. Il risultato più rilevante è quello di una riduzione della mortalità assoluta del 9%».Questo studio è stato il primo nel mondo occidentale sull'utilizzo del plasma convalescente nella terapia anti Covid. Si apriva un concreto spiraglio di speranza. Immediatamente sui due ospedali sono arrivate richieste a valanga per avere i dettagli della terapia. Gli Stati Uniti sono stati primi a muoversi, autorizzando subito a utilizzare il plasma di soggetti in convalescenza da Covid come terapia emergenziale assieme al remdesivir. Ma in Italia la comunità scientifica si è divisa tra i fautori e i contrari. Questi ultimi hanno riesumato vecchie polemiche sui rischi dell'uso del plasma e sulla mancanza di un'evidenza scientifica definitiva, che però è possibile solo dopo una lunga sperimentazione.Altre perplessità si aggiunsero quando apparvero ricerche come quella condotta dall'Indian council of medical research secondo cui il plasma iperimmune non riduce la mortalità Covid e non ha effetti rilevanti sul decorso della malattia: ricerche poi rivelatesi prive di fondamento scientifico. Forti critiche si abbatterono sui due ospedali lombardi. Tra gli altri, il dottor Giuseppe De Donno, primario di pneumologia a Mantova, divenne un volto noto nel difendere e spiegare la bontà del metodo. Nel frattempo, gli ospedali d'oltralpe chiamavano i colleghi di Pavia e Mantova per imparare e poter applicare la loro cura. All'estero, dunque, la terapia lombarda va alla grande. E in Italia, che fine ha fatto? Al momento manca l'autorizzazione dell'Aifa, che arriva quando sul farmaco c'è un'evidenza scientifica definitiva. Le Regioni si muovono in ordine sparso creando banche del plasma. L'Aifa ha promosso uno studio nazionale denominato Tsunami, con l'obiettivo, come spiega alla Verità, di «valutare con opportuno rigore metodologico l'efficacia e la sicurezza della terapia. Ma non prevede in alcun modo un trattamento industriale del plasma».A oggi hanno aderito al programma 76 centri, ma ne sono stati attivati soltanto 15 e in appena 8 sono iniziati gli arruolamenti di pazienti: 7 in Toscana più Niguarda a Milano. Dal 15 luglio, soltanto 34 pazienti sono stati trattati con questa sperimentazione; il paziente 1 è guarito in 72 ore con la comparsa di anticorpi prima mancanti. L'Aifa però ammette che «non è possibile al momento prevedere quando sarà completato l'arruolamento e quando saranno disponibili i primi dati». Per stilare una prima analisi preliminare servono 250 pazienti e per la validità scientifica bisogna arrivare a 476: così ha spiegato il dottor Francesco Menichetti, direttore dell'unità malattie infettive dell'ospedale di Pisa. Il quale conferma che, di fatto, è tutto fermo.È molto probabile che ci vorrà ancora molto tempo per avere risultati definitivi. Come bisognerà aspettare almeno un paio d'anni per avere un farmaco. In Italia c'è un'unica azienda del settore dei plasmaderivati, tra le prime cinque al mondo, la toscana Kedrion, appartenente alla famiglia Marcucci, che potrebbe arrivare a produrre un medicinale apposito. «Stiamo lavorando a un farmaco con immunoglobuline iperimmuni. Non utilizziamo il plasma nella sua totalità ma solo gli anticorpi contenuti, che sono quindi concentrati e sterilizzati. Il farmaco potrebbe essere utilizzato anche in soggetti sani. Avrebbe una durata inferiore al vaccino, circa uno o due mesi, e i soggetti sarebbero immunizzati temporaneamente. La vaccinazione fornisce una protezione di lunga durata», spiega Alessandro Gringeri, responsabile ricerca e sviluppo di Kedrion, «ma non si può effettuare su soggetti malati o immunodepressi. Il farmaco con le immunoglobuline potrebbe servire per le emergenze, per situazioni acute o per pazienti affetti con sintomatologia lieve, che sta evolvendo». Quali sono i tempi? «Ora stiamo facendo la sperimentazione in Israele», risponde Gringeri, «in collaborazione con l'azienda israeliana Kamada e contiamo di inoltrare la richiesta di approvazione entro la fine del prossimo anno. Nel 2022 il farmaco potrebbe essere sul mercato».<div class="rebellt-item col1" id="rebelltitem1" data-id="1" data-reload-ads="false" data-is-image="True" data-href="https://www.laverita.info/insabbiata-lunica-cura-antivirus-che-funziona-2648169879.html?rebelltitem=1#rebelltitem1" data-basename="noi-abbiamo-scoperto-la-terapia-pero-sono-gli-altri-ad-applicarla" data-post-id="2648169879" data-published-at="1602444911" data-use-pagination="False"> «Noi abbiamo scoperto la terapia però sono gli altri ad applicarla» Cesare Perotti «L'Italia scopre la terapia ma poi sono gli altri che la applicano su larga scala. Mentre la comunità scientifica italiana si divideva tra favorevoli e contrari, gli Stati Uniti hanno preso la nostra terapia e, senza perdere tempo, la stanno utilizzando su tutto il territorio nazionale. Anche numerosi Paesi europei ce l'hanno chiesta». Cesare Perotti è direttore del servizio immunotrasfusionale del policlinico di Pavia, che per primo assieme all'ospedale Carlo Poma di Mantova ha sperimentato la terapia del plasma iperimmune per curare i malati da Covid. È vero che la vostra cura è stata copiata dagli Stati Uniti? «Il 18 marzo mi ha telefonato la presidente dell'American society of hematology. È stata molto diretta. Mi ha chiesto se potessi mandarle il protocollo che avevamo elaborato per la cura con il plasma iperimmune. Ho risposto subito. Negli Usa il programma è partito immediatamente. La Food and drug administration, l'ente governativo che regolamenta i prodotti alimentari e farmaceutici, dipendente dal Dipartimento della salute, ha autorizzato l'utilizzo del plasma di soggetti in convalescenza da Covid, come terapia emergenziale insieme al Remdesivir, un farmaco antivirale». Quanti pazienti sono stati trattati negli Usa con la vostra cura? «Il sito della Mayo Clinic, che coordina tutto il programma negli Stati Uniti, riporta i dati aggiornati sull'applicazione della terapia. Sono coinvolti 2.747 ospedali, 14.759 medici partecipano al programma e hanno avuto l'infusione 85.206 malati. Il presidente Donald Trump, da quanto si è saputo, è stato curato con anticorpi monoclonali alcuni ottenuti dal plasma, altri realizzati in laboratorio». Quali altri Paesi si sono rivolti a voi? «Il Policlinico ha dato il protocollo anche a Francia e Spagna». Le istituzioni europee si sono mosse? «La Commissione ha assegnato al policlinico San Matteo di Pavia e a me il coordinamento del programma del plasma convalescente per l'Europa con un finanziamento che coinvolge tutti i Paesi europei. Con il programma European blood alliance abbiamo avuto un importante riconoscimento oltre confine». Quale è la situazione in Italia? «Ci muoviamo tra tante polemiche. Ci hanno criticato perché quando siamo partiti a marzo non avevamo risultati randomizzati. Ma questi richiedono molto tempo e a marzo, in piena pandemia, non potevamo aspettare: dovevamo agire subito e i risultati sono stati ottimi». Quando sarà ufficializzata la cura? «A fine maggio è partito lo studio chiamato Tsunami, coordinato da me e dall'ospedale di Pisa. È un protocollo nazionale randomizzato, promosso dal ministero della Salute, dall'Istituto superiore di sanità e dall'Aifa, con l'obiettivo di ottenere evidenze scientifiche sul ruolo della terapia con il plasma iperimmune. Hanno aderito 76 ospedali, ma un conto è iscriversi e un altro attivarsi. Si procede lentamente. D'altronde i convalescenti a cui fare i prelievi sono diminuiti e l'arruolamento di pazienti va a rilento. Dovevamo partire prima». Come mai non è stato attivato subito un programma nazionale? «C'è stato un deficit di organizzazione e tante, troppe, polemiche». A pensare male talvolta ci si indovina: non è che questa terapia, siccome ha costi ridotti, dà fastidio all'industria farmaceutica? «Pasolini diceva: io so ma non ho le prove. Una cura con l'eparina o il desametasone che costa 2-3 euro impatta in modo diverso rispetto a un antivirale come il Remdesivir che costa circa 2.500 euro a paziente». C'è al mondo una terapia standard per la cura del Covid? «La risposa è no. Ci sono evidenze che alcuni approcci terapeutici vanno meglio di altri. Per la cura del Covid si usano diversi farmaci, ognuno per la sua specificità». Ogni tanto appare uno studio che contesta l'efficacia della cura con il plasma, per esempio quello dell'Indian council of medical research. «È uno studio che non ha alcuna validità. Hanno preso del plasma a caso, senza effettuare i test preventivi in grado di verificare se ci fossero gli anticorpi. Di che cosa stiamo parlando?». <div class="rebellt-item col1" id="rebelltitem2" data-id="2" data-reload-ads="false" data-is-image="True" data-href="https://www.laverita.info/insabbiata-lunica-cura-antivirus-che-funziona-2648169879.html?rebelltitem=2#rebelltitem2" data-basename="a-mantova-le-guarigioni-superano-il-90" data-post-id="2648169879" data-published-at="1602444911" data-use-pagination="False"> «A Mantova le guarigioni superano il 90%» Massimo Franchini «Avremmo dovuto agire subito ma c'è stata una forte resistenza dovuta al pregiudizio che si porta dietro l'uso del plasma. È vero, fino a 40 anni fa poteva trasmettere l'epatite e l'Hiv, ma ora è super testato e questi rischi si sono annullati». Massimo Franchini, direttore del servizio di immunoematologia e medicina trasfusionale dell'ospedale Carlo Poma di Mantova, che per primo ha avviato la sperimentazione della terapia con il plasma iperimmune, rivela come mai in Italia la cura fa fatica a essere accettata. «A marzo e aprile ci fu molta resistenza dalla comunità scientifica. Forse ha giocato anche il solito meccanismo del campanilismo di qualche scienziato che avrebbe voluto mettere il suo nome sotto la cura. Ma i risultati ci sono. Noi siamo stati i primi nel mondo occidentale a individuare questa terapia. Il paradosso è che è stata utilizzata soltanto da pochi centri che ci hanno creduto. Adesso, in tutto il mondo, sono in corso centinaia di studi sul plasma iperimmune. In Italia invece si reagisce quasi con gioia quando esce qualche lavoro che mette in dubbio l'efficacia della terapia». Lei è responsabile della sicurezza del plasma: come mai tanta reticenza a usare una cura che altri Paesi ci hanno copiato? «È proprio questo il punto. Il plasma che usiamo è super sicuro, non c'è alcun rischio di trasmettere malattie infettive. Inoltre, si sa quanti anticorpi contiene come se fosse un farmaco. Calcoliamo il numero di dosi, quanto e come somministrarlo. Ma poi, basta pensare che personaggi come Trump e Berlusconi sono stati trattati con un mix di farmaci che comprendeva il cortisone come antinfiammatorio, il remdesivir come antivirale e anche una fonte di anticorpi come i monoclonali o il plasma iperimmune». Bisognerebbe creare delle banche del plasma, ma manca una regìa pubblica e tutto è lasciato all'iniziativa degli ospedali. «Ci sarebbe voluto un maggior coordinamento dell'Istituto superiore di sanità per la raccolta di plasma. Gli Usa sono partiti subito con la nostra terapia, tramite una task force governativa che ha promosso la raccolta di plasma su tutto il territorio nazionale. L'Italia è stata interessata precocemente dalla pandemia ma si è mossa lentamente. Ci sono banche del plasma regionali in Lombardia, Veneto, Toscana, Marche, Lazio, legate agli ospedali. L'utilizzo clinico è coordinato dallo studio Tsunami». Quando dalla sperimentazione si passerà a un uso su larga scala? «Sì, al momento siamo ancora alla sperimentazione. L'Aifa autorizza i farmaci e le terapie quando ci sono prove scientifiche definitive, che nel nostro caso ancora non ci sono. Per averle occorre un processo lungo che richiede tanto tempo. Ma la mia opinione è che una volta appurata la sicurezza e a fronte dei risultati ottimi della sperimentazione, perché non usarlo? Gli americani si sono posti questa domanda e, con grande pragmatismo, hanno deciso di adottare la terapia anche senza evidenze scientifiche definitive». Avete posto questo problema all'Istituto superiore di sanità? La pandemia richiede interventi tempestivi. «L'Istituto è stato interpellato più volte, ma secondo loro non valeva la pena di usare il plasma in modo estensivo. Hanno dubbi sull'efficacia, hanno sempre mantenuto questa linea. La storia della medicina dirà chi aveva ragione». In attesa dell'autorizzazione degli istituti sanitari, come potete applicare la terapia? «La cura del plasma è inserita in protocolli di studi, come lo Tsunami, o per cosiddetto uso compassionevole, cioè quando per una patologia manca un trattamento riconosciuto come definitivo ma si ritiene che un farmaco possa essere utile. Occorre l'autorizzazione del Comitato etico che noi abbiamo». Quali risultati avete ottenuto nell'ospedale di Mantova? «Stiamo applicando la terapia da marzo e finora abbiamo trattato 150 pazienti. Le guarigioni superano il 90%». Ci sono requisiti affinché il plasma abbia la maggiore efficacia? «Il plasma funziona se vengono rispettati i seguenti requisiti: deve contenere un adeguato livello di anticorpi e deve essere somministrato precocemente. Con queste condizioni la malattia si blocca e regredisce». Avete ricevuto richieste da Paesi esteri per fornire supporto scientifico? «Abbiamo continue richieste di collaborazioni per mettere a disposizione le nostre conoscenze. Abbiamo fornito un supporto scientifico con collegamenti Web dall'America Latina all'Albania». Siete un competitor temibile per l'industria farmaceutica. La cura con il plasma costa poco. «Qualcuno ci può considerare un pericoloso competitor, ma io vedo un rapporto di collaborazione e non di antagonismo con l'industria farmaceutica. La terapia migliore, al momento, è un cocktail di componenti, quali antivirali, cortisone e plasma. La produzione di un farmaco richiede tanto tempo e forse per quella data sarà già arrivato il vaccino».
Il baritono Luca Salsi ci guida alla scoperta del genio di Giuseppe Verdi attraverso tre opere che lo vedono protagonista al Teatro alla Scala di Milano. Da Nabucodonosor, primo grande successo del Cigno di Busseto, al penultimo capolavoro, Otello. Un titolo attesissimo per l’inaugurazione della prossima stagione, il 7 dicembre 2026.
Un duello tra Lautaro Martinez e Scott McTominay durante Inter-Napoli della scorsa stagione (Getty Images)
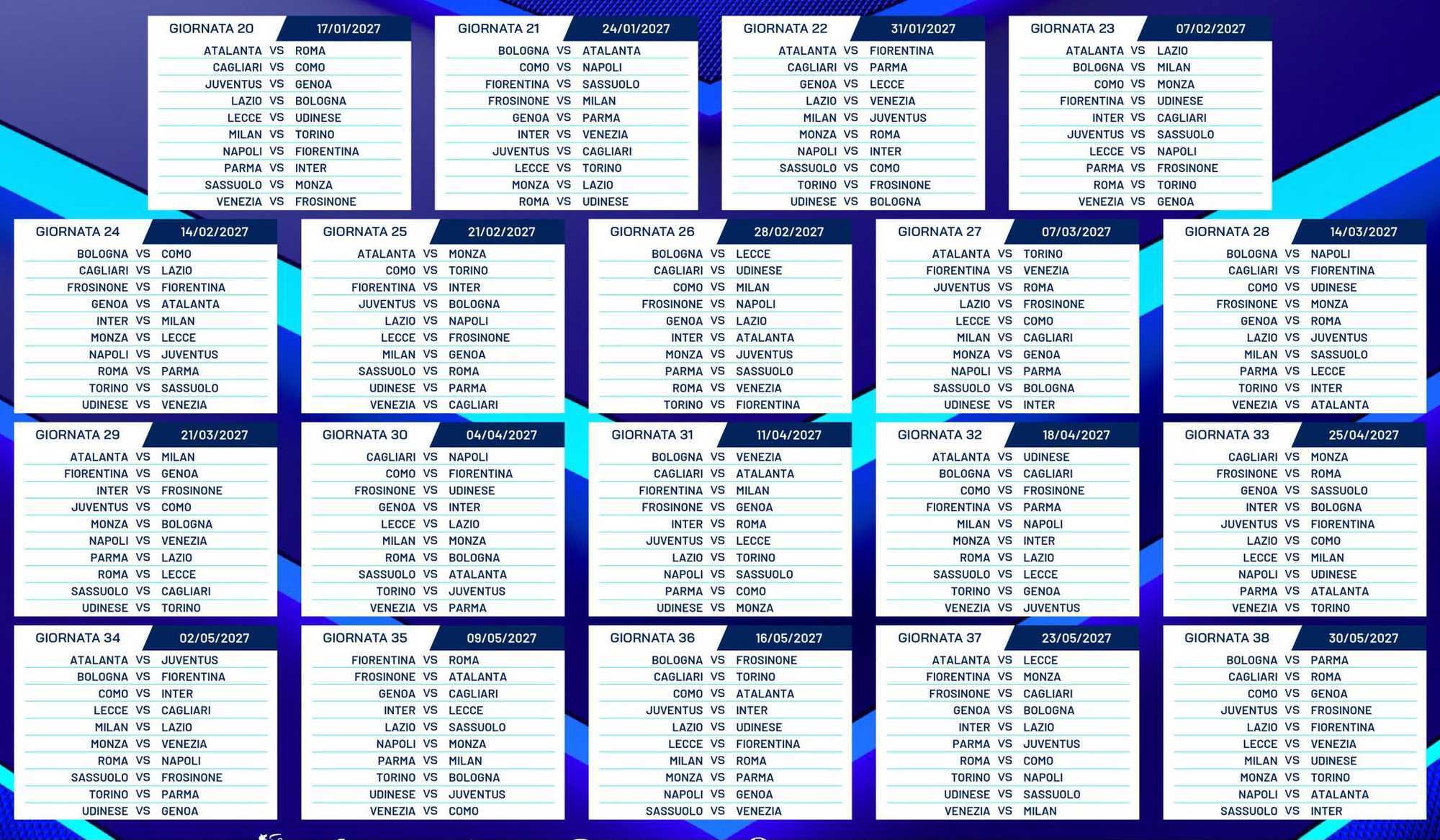
A nemmeno due settimane di distanza dalla fine del campionato, la Serie A versione 2026/2027 ha già preso forma con la tradizionale compilazione del calendario. Per il secondo anno consecutivo il Teatro Regio di Parma, nell'ambito del Festival della Serie A, ha ospitato la cerimonia che ha svelato le 38 giornate della prossima stagione.
Il campionato scatterà nel weekend del 22-23 agosto e si concluderà il 29-30 maggio 2027. Confermato il calendario asimmetrico tra andata e ritorno, mentre la principale novità riguarda le soste per le nazionali: tra fine settembre e inizio ottobre ci sarà una pausa unica di due settimane consecutive, alle quali si aggiungeranno gli stop di novembre e marzo. Previsti inoltre due turni infrasettimanali, il 28 ottobre e il 6 gennaio, oltre alla sosta natalizia del 26 e 27 dicembre.

L'avvio propone subito partite interessanti e affatto banali. I campioni d'Italia dell'Inter debutteranno a San Siro contro il Monza, mentre Napoli e Juventus inizieranno entrambe in trasferta, rispettivamente a Genova e Frosinone. Impegno esterno anche per il Milan, atteso dal Torino, mentre la Roma riceverà la Fiorentina all'Olimpico. Per assistere ai primi incroci di alta classifica non bisognerà però aspettare molto. Già alla terza giornata il calendario mette di fronte Juventus e Milan da una parte, Inter e Napoli dall'altra. Un doppio confronto che potrebbe offrire indicazioni interessanti fin dalle prime settimane della stagione. Il primo derby della Madonnina è invece fissato alla decima giornata, il 1° novembre, nello stesso turno in cui andrà in scena anche Juventus-Napoli. Al termine del girone d'andata, alla diciannovesima giornata, spazio al primo Derby d'Italia con Inter-Juventus a San Siro.

Anche il ritorno si annuncia particolarmente intenso. Alla ventiduesima giornata si giocheranno Napoli-Inter e Milan-Juventus, mentre due settimane più tardi, nel weekend di San Valentino, il calendario propone un altro doppio appuntamento di cartello con Inter-Milan e Napoli-Juventus. Restano inoltre i vincoli legati agli impegni europei. Nelle giornate collocate tra due turni delle coppe Uefa le squadre impegnate in Champions League non potranno affrontare quelle partecipanti a Europa League e Conference League, una scelta pensata per distribuire in modo più equilibrato gli impegni durante la stagione.
Dietro la compilazione delle 38 giornate c'è stato ancora una volta il lavoro dell'algoritmo utilizzato dalla Lega Serie A, chiamato a gestire contemporaneamente decine di vincoli tra derby, alternanza casa-trasferta, soste per le nazionali, coppe europee e disponibilità degli impianti. Un supporto tecnologico ormai diventato centrale nella costruzione del calendario. Ad aprire la cerimonia è stato il presidente della Lega Serie A, Ezio Simonelli, che ha rivendicato la crescita dell'interesse attorno al campionato sottolineando: «Abbiamo avuto una capienza media negli stadi di 30.000 spettatori a partita. La prova che il pubblico ama ancora e molto il nostro campionato».
Continua a leggereRiduci
Giuseppe Cossu e Roberto Saviano (Ansa)
Caro Roberto Saviano,
ho letto le tue parole sul grido “Decima” pronunciato dagli incursori della Marina Militare e sento il bisogno di scriverti da uomo che ha servito l’Italia in uniforme, in patria e all’estero, compreso l’Afghanistan. Non per polemica, ma per offrire un punto di vista che troppo spesso viene ignorato.
Chi ha indossato il basco degli incursori sa bene che la storia va conosciuta nella sua interezza, senza semplificazioni e senza sovrapposizioni che finiscono per cancellare fatti, uomini e tradizioni. Quando sento pronunciare il nome “Decima”, il mio pensiero non corre alla Repubblica Sociale Italiana né alle pagine più controverse della guerra civile italiana. Corre invece agli uomini della Decima Flottiglia MAS che, prima dell’8 settembre 1943, scrissero alcune delle pagine più straordinarie della storia militare italiana.
Parlo di marinai che operarono in condizioni estreme, di pionieri delle operazioni speciali subacquee, di uomini che con mezzi rudimentali ma con coraggio eccezionale riuscirono a colpire obiettivi ritenuti impossibili. Parlo di una tradizione professionale e militare riconosciuta e studiata ancora oggi da numerose marine del mondo. È da quella tradizione tecnica, operativa e umana che discendono gli attuali incursori della Marina Militare.
Quando pensiamo a quella storia, pensiamo al sacrificio di Teseo Tesei e di tanti altri uomini che hanno rappresentato e continuano a rappresentare un esempio per ogni incursore. Pensiamo a chi ha dato la vita per compiere il proprio dovere, sapendo di andare incontro a una missione dalla quale forse non sarebbe tornato. Il loro esempio continua ancora oggi a essere fonte di motivazione nelle notti più dure dell’addestramento e delle operazioni.
Pensiamo anche alle radici più profonde dello spirito d’audacia della Marina italiana, a imprese come la Beffa di Buccari guidata da Gabriele D’Annunzio, episodi che hanno alimentato una tradizione fatta di coraggio, iniziativa e spirito di sacrificio. Sono queste le pagine che molti giovani militari studiano, insieme ai valori e ai principi tramandati dal reparto, trovando ispirazione per affrontare le sfide del servizio.
Ridurre tutto questo a una sola fase storica significa compiere un’operazione ingiusta nei confronti della verità. Significa ignorare che la Decima MAS esistette prima del 1943 e che proprio in quel periodo costruì la propria fama. Significa dimenticare uomini che servirono il loro Paese con disciplina e sacrificio in un contesto storico ben diverso da quello successivo all’armistizio.
C’è poi una domanda che mi pongo sinceramente: perché soltanto oggi questa tradizione viene presentata come un problema? Il grido “Decima” accompagna da sempre la storia e le tradizioni del reparto. Nel corso dei decenni si sono succeduti governi di ogni orientamento politico, presidenti della Repubblica, ministri della Difesa e vertici militari. Eppure nessuno ha mai ritenuto necessario trasformare questo elemento identitario in una battaglia ideologica.
Noi militari conosciamo il peso dei simboli. Proprio per questo sappiamo distinguerne le diverse fasi storiche. Nessuno pretende di cancellare le controversie che seguirono all’8 settembre. Ma allo stesso modo non si può accettare che un’intera tradizione venga identificata esclusivamente con una parte della sua storia, per quanto discussa essa sia.
Molti di coloro che oggi rivendicano l’eredità professionale degli incursori italiani hanno servito la Repubblica Italiana in missioni internazionali, spesso lontano dai riflettori. In Afghanistan, nei Balcani, in Iraq, nel Mediterraneo, nel Corno d’Africa e in numerosi altri teatri operativi, i militari italiani hanno operato per garantire sicurezza, stabilità e protezione delle popolazioni civili, spesso a rischio della propria vita.
Ho visto colleghi partire senza sapere se sarebbero tornati. Ho visto uomini lavorare per mesi lontano dalle famiglie, affrontando minacce concrete e quotidiane. Ho visto professionalità, umanità e spirito di servizio. E ho visto il rispetto che i militari italiani si sono guadagnati presso alleati e popolazioni locali grazie alla loro competenza e al loro equilibrio.
Quando un incursore richiama una tradizione militare, non necessariamente sta facendo una dichiarazione politica. Molto spesso sta rendendo omaggio a una storia professionale fatta di addestramento, sacrificio, fratellanza e servizio. È una differenza che chiunque affronti questi temi con onestà intellettuale dovrebbe sforzarsi di comprendere.
Se vi sono critiche da rivolgere a un governo, a una maggioranza politica o a una scelta istituzionale, esse appartengono legittimamente al dibattito democratico. Ma sarebbe auspicabile evitare che a farne le spese siano uomini che hanno dedicato la propria vita alla difesa della Patria e delle sue istituzioni. Militari che servono tutti gli italiani, senza distinzione di idee politiche, religione, origine o appartenenza sociale.
Le parole hanno un peso, soprattutto quando vengono pronunciate da personalità pubbliche. Per questo credo che sia importante distinguere tra la doverosa critica politica e il rispetto dovuto a chi serve lo Stato italiano. Le semplificazioni possono generare consenso immediato, ma raramente aiutano a comprendere la complessità della storia.
E forse, anziché soffermarsi esclusivamente sugli aspetti più controversi di quella vicenda, sarebbe utile raccontare anche le imprese che hanno reso celebre la Decima nel mondo: il coraggio di Teseo Tesei, le operazioni degli uomini d’assalto, l’innovazione tecnica, il sacrificio e la dedizione di chi ha aperto la strada alle moderne forze speciali. Sarebbe una storia capace di offrire ai nostri giovani esempi di determinazione, spirito di servizio e amore per il proprio Paese.
Non ti chiedo di condividere questa sensibilità. Ti chiedo soltanto di considerare che dietro quel nome, per molti militari, non vi è nostalgia ideologica, bensì il ricordo di una tradizione operativa che appartiene alla storia della Marina italiana e che ha contribuito a costruire l’eccellenza delle nostre forze speciali.
La storia, quando viene letta tutta intera, è sempre più complessa degli slogan. E il rispetto per chi ha servito e serve il proprio Paese dovrebbe essere un terreno comune, al di là delle differenze di opinione.
Con rispetto.
Giuseppe Cossu, Incursore in congedo della Marina Militare italiana.
Continua a leggereRiduci